داروی جدیدی که یک تنه به جنگ همه ویروسها خواهد رفت

یکی از خبرهای داغی که هفته پیش خواندم، خبر مربوط به کشف داروی ضد ویروس جدیدی بود که میتواند علیه همه ویروسهای مورد استفاده قرار بگیرد.
نویسندگان مهمان یک پزشک در این پست در مورد این دارو و کشف جدید توضیح میدهند:
توضیح در مورد این دارو را سروش شروع میکند:
از سال 1918 که «ویکتور فلمینگ»، پنیسیلین را به طور تصادفی هنگام مطالعه نوعی قارچ کشف کرد، تحول بزرگی در پیشگیری و درمان بیماریهای عفونی ایجاد شد و امید به زندگی بین انسانها به طور قابل توجهی افزایش پیدا کرد. اما پنیسیلین و سایر آنتیبیوتیکها تنها روی باکتریها، انگلها و قارچها موثرند و درمان بیماریهای ویروسی مثل ایدز، هپاتیت و حتی سرماخوردگی همواره با مشکل روبرو بوده است.
داروهای ضد ویروس تنها روی یک ویروس یا یک خانواده از ویروسها مؤثرند. به علاوه ایجاد جهش ژنتیکی در ویروسها سبب مقاومت دارویی در آنها میشود. اپیدمیهای سارس و آنفولانزای H1N1 در سالهای اخیر به دلیل فقدان داروهای ضد ویروس مناسب با اثرگذاری کامل علیه این بیماریها و همچنین الگوی ساده انتقال انسان به انسان در آنها رخ داد.
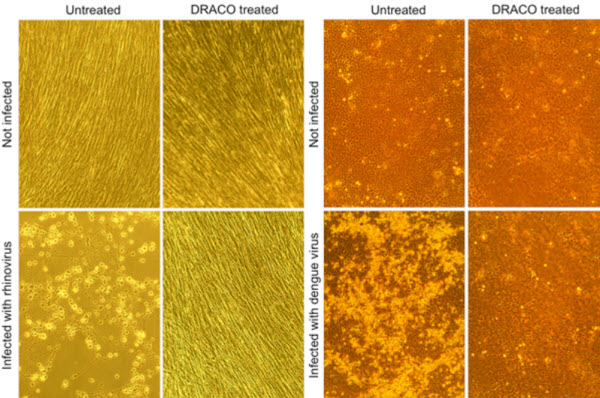
پژوهشگران دانشگاه MIT اخیرا موفق به کشف یک داروی ضد ویروس جدید با قدرت تأثیر بالا شدهاند که اثری مشابه اثر آنتیبیوتیکها روی باکتریها دارد. این دارو از طریق تحریک آپوپتوز یا مرگ برنامهریزی شدهی سلول آلوده به ویروس سبب از بین رفتن عفونت میشود. این درمان در سلولهای حیوانی و انسانی در محیط آزمایشگاه٬ بر روی 15 ویروس مختلف از جمله سرماخوردگی٬ آنفولانزای H1N1 ، فلجاطفال٬ تب دانگ و انواع مختلفی از تبهای خونریزیدهنده بررسی شده و مؤثر بوده است، اما از نظر تئوریک می تواند روی هر بیماری ویروسی عمل کند.
ویروسها پس از آلوده کردن سلولها٬ با استفاده از امکانات آن DNA یا RNA خود را کپیبرداری کرده و علاوه بر آن که سبب مرگ سلول میشوند، خود را تکثیر میکنند. مکانیسم دفاعی بدن در مقابل ویروسها، تولید پروتئینهایی است که به RNA دورشتهای ویروس متصل شده و مانع کپیبرداری آن می شوند. این روش درمانی بر اساس استفاده از ترکیبی از این پروتئینهاست که بطور مختصر DRACO یا double-stranded RNA activated caspase oligomerizers نامیده میشود. یک انتهای DRACO به RNA دورشتهای ویروس متصل میشود و انتهای دیگر آن موجب تحریک آپوپتوز و مرگ سلول پیش از تکثیر ویروس میشود.
DRACO سبب بهبود یک موش آزمایشگاهی مبتلا به آنفولانزا H1N1 شدهاست و پژوهشگران امیدوارند به کمک آن مانع ایجاد اپیدمیهای گسترده مثل آنفولانزا شوند. گرچه برخی پزشکان در مورد موفقیت عملی آن تردید دارند. مرگ تعداد زیادی سلول و آزاد شدن فراوردههای سلولی و بهمخوردن سطح سرمی الکترولیتها در موارد استفاده از این دارو در عفونتهای ویروسی شدید٬ میتواند اثرات بالینی خطرناکی داشته باشد.
برخلاف آنتیبیوتیکها احتمال ایجاد مقاومت میکروبی در برابر دارو٬ که به دلیل استفاده بی رویه و نادرست ایجاد می شود٬ در مورد DRACO کم است و میتوان آن را با خیال آسودهتر استفاده کرد. این دارو میتواند گام مهمی در پیشگیری از بروز اپیدمیهای ویروسی و درمان جدیدی برای بیماری هپاتیت و ایدز باشد. حتی ممکن است به کمک آن و با خوردن چند عدد قرص بتوان از شر سرماخوردگی در زمستانها خلاص شد. اما برای اطمینان از نتایج بالینی استفاده از این دارو باید منتظر طی مراحل تحقیقاتی و بررسی گسترده اثرات آن در حیوانات آزمایشگاهی و سپس انسان باشیم.
در ادامه برای دوستانی که میخواهند تخصصیتر در مورد DRACO بدانند، توضیحات بهروز قنبری را اضافه میکنم:
در روش دراکو، دو پروسه طبیعی سلولی ترکیب شدهاند:
اولین پروسه مرتبط با شناسایی RNA دو رشتهای است. بیشتر ویروسها ژنوم RNAی دورشتهای (dsRNA) یا تک رشتهای (ssRNA) دارند وباقی ویروسها ژنوم DNA دارند که معمولا در رونویسی نامتقارن، RNA دو رشتهای بلند تولید میکنند در حالی که این امر در سلولهای پستانداران رخ نمیدهد یعنی RNA دو رشتهای بلند (بلندتر از 23-21 جفت باز) تولید نمیکنند. دفاع طبیعی سلولی جهت مقابله با عفونتهای ویروسی این تفاوت را شناسایی مینماید. برای مثال پروتئین کاینیز R (PKR) در سمت N-ترمینال خود (انتهای آمین یک رشته پروتئینی) دو موتیف (جایگاه) برای اتصال به dsRNA هایی با طول حداقل 50-30 جفت باز دارد. با اتصال به dsRNA این آنزیمها خود را فسفریله میکنند و به این ترتیب فعال میشوند. PKR فعال به نوبه خود eIF-2a را فسفریله میکند که فاکتور آغاز رونویسی در یوکاریوتها است و با فسفریله شدن غیر فعال میشود و به این ترتیب مانع رونویسی پروتینهای ویروسی و سلولی میگردد. (پروتئین های دیگری هم در سلول وجود دارند که همانند PKR، RNA دورشتهای را شناسایی میکنند)
فرآیند طبیعی دوم که برای ساخت دراکو استفاده شده است در واقع یکی از مراحل آخر مسیر آپوپتوز است که طی آن کمپلکسهای حاوی مولکولهای سیگنالینگ درون سلولی مرتبط با آپوپتوز مانند Apaf-1 ( فاکتور فعال کننده پروتئاز آپوپتوتیک 1) یا ناحیه مرگ فعال شده توسط FLICE با عنوان FADD همزمان به چندین پروکاسپاز متصل می شوند و آنها را برش میدهند، در اثر این برش پروکاسپازها فعال میشوند و سایر کاسپازهای زنجیره را فعال مینمایند که آنها نیز باعث برش دادن (از کار افتادن) طیفی از پروتئینهای سلولی و نهایتا مرگ سلول میشوند.
در حالت طبیعی بسیاری از ویروسها با هدف گرفتن پروتئینهای مسیر شناسایی dsRNA سیستم دفاعی میزبان را دور میزنند. برخی ویروسها مانند poxvirus هم تلاش میکنند dsRNA را جدا نگه دارند و یا در نواحی متصلشونده به dsRNA در پروتئینهای سلولی اختلال ایجاد کنند، مانند ویروس ایدز.
نکته مهم این است که تقریبا همه ویروسها در مراحل اول آپوپتوز سلول را از چنگ مرگ فراری می دهند. دراکو با القای خودکشی سلولی مانع این عمل میشود.
به زبان ساده DRACO یک پروتئین کایمری (ترکیبی) است که از یک سمت خود به RNA دو رشتهای ویروس متصل شده و سمت دیگر آن یک پروکاسپاز است که هنگام اتصال دراکو ها با dsRNA ویروسی فعال شده و مرگ سلولی (آپوپتوز) را القا می کند که طی آن سلول همراه با ویروس به کام مرگ فرستاده میشود. اگر dsRNA درون سلول نباشد دراکوها فعال نخواهند شد و آپوپتوز رخ نمیدهد.
در شکل زیر میتوانید تصویر شماتیک چند نمونه از دراکوهای ساختهشده را ببینید. در همه دراکوها ناحیه اتصال به RNA دورشتهای (قرمز)، ناحیه القای آپوپتوز (سبز و آبی) و دو ناحیه زرد رنگ یکی تگ پروتئینی (هیستیدین تگ) به منظور خالصسازی پروتئین دارویی پس از تولید و دیگری جهت ورود (ترانسداکشن) دراکو به سیتوپلاسم وجود دارد:

دراکو یک نمونه از کاربرد مهندسی پروتئین در بیوتکنولوژی مدرن است که مستلزم دانش دقیق از ساختمان و عملکرد پروتئینهاست در اینجا از اتصال نواحی عملکردی دو پروتئین متفاوت جهت خلق یک داروی ضد ویروسی وسیعالطیف استفاده شده است. یک نمونه دیگر از کاربرد مهندسی پروتئین در پزشکی داروی ریلوناسپت (Rilonacept) با نام تجاری آرکالیست (Arcalyst) است که حاوی ناحیه خارج سلولی گیرنده اینترلوکین 1 انسانی (IL-1) و ناحیه FC (دم آنتیبادی که به گیرندههای سطح سلول متصل می شود) IgG1 انسانی است. این پروتئین با اتصال به اینترلوکین 1 آن را خنثی میکند و در درمان طیفی از بیماریهای خود التهابی کاربرد دارد.
منابع: newscientist – healthland– plosone

خیلی عالیه ! قسمتای تخصصی شو که نفهمیدیم :دی
ممنون
واقعا مطلب جالبی بود !
فکر کنم اولین سوالی که برای خواندگانی که تخصصی در علم پزشکی ندارند پیش بیاد این موضوع باشه که روند تحقیق و بررسی این کشف برای اینکه به تولید انبوه برسه چقدر ممکن است طول بکشد ؟
Kheili mamnoon!
دست شما و نویسنده های مهمان درد نکنه. خیلی عالی بود .
ویکتور فلمینگ کارگردان سینماست!!!!
نام درست الکساندر فلیمینگ است
خیلی جالب بود. مخصوصاً قسمتی که روش دراکو رو توضیح داده بود 🙂
واقعا عالی بود.ممنون.